
トップページ >>がんの代替医療における有効症例の調査研究
がんの代替医療における有効症例の調査研究
厚生労働省がん研究助成金「がんの代替医療の科学的検証に関する研究」班では、
健康食品などをはじめとした民間療法(以下、「代替医療(だいたいいりょう)」と言います)に関して、安全性と有効性を検証する研究に取り組んでいます。 現在、情報技術の発達によって、がん患者さんやその家族の方々は、がんの代替医療に関する情報を、大量に目にしたり耳にしたりしています。しかし、その情報の信憑性や正確性については不確実であるのが現状です。
そこで、今回、それらの情報について第三者的立場で厳密に審査する取り組みを研究班の研究として計画しました。今回の取り組みは、診療録等診療情報を収集・集計して行う観察研究(臨床の場における疫学研究)となります。
代替医療の研究に関して積極的に取り組んでいる米国においても、国立がん研究所が今回研究班が行う取り組みと同様のBest Case Series Programに取り組んでいます(http://www.cancer.gov/cam/bestcase_intro.html)。
先生方におかれましては、日々の診療でお忙しいとは思いますが、本研究の主旨をご理解頂き、代替医療が有効であったと推測される患者さんの医療情報の提供にご協力を賜りたくお願い申し上げます。なお、本研究は倫理委員会の審査を受け承認を得ています。
※本研究は、平成22年度より、がん研究開発費「がんの代替医療の科学的検証に関する研究」班(主任研究者:山下素弘)の研究の一環として行われています。
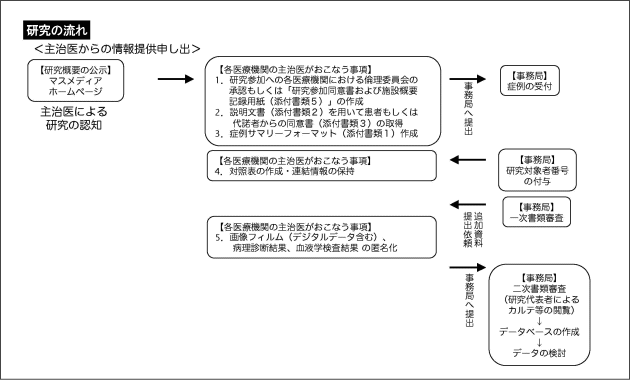
研究の流れ
代替医療が有効であったと推測される患者さんの医療情報は、以下のような流れで審査されていきます。
【評価対象項目】
1.抗腫瘍効果
<悪性固形腫瘍の場合>
Response Evaluation Criteria In Solid Tumors (RECIST) 基準においてComplete response (CR)、Partial response(PR)、Stable disease (SD)を審査対象とする
<悪性血液腫瘍>
Complete remission (CR)のみを審査対象とする。
2.QOL改善、症状の緩和など
血液検査値、質問票(一般的に研究用と認知されたもの)等の客観的指標によって評価されている場合のみ対象とする。
①
一次書類審査
患者さんの主治医もしくは代替医療を実践している医師等が、今までの患者さんの治療経過をまとめた症例サマリーフォーマット(様式は以下からダウンロード可能)を作成し提出
<<書類提出先および当該研究に関する問い合わせ先>> 〒162-0041 東京都新宿区早稲田鶴巻町513 |
以下の手順に従いまして資料の提出をお願い致します。
- 先生の施設用の 同意書 にご署名頂き、当方へ提出してください。
- 説明文書 を用いて患者に本研究の主旨をご説明頂き、同意書 を取得してください。
なお、患者様が同意を撤回された場合は、同意撤回文書 をご使用ください。
- 症例サマリーフォーマット を留意点に従ってご記入頂き、当方へ提出してください。
※なお、ご記入にあたっては、記入例 をご参照ください。
ご不明な点がございましたら、研究代表者(大野)までご連絡ください。
![]()
今回、この研究へ参加を希望される場合は、まず主治医の先生にこの研究についてお話をしてみてください。
また、対象者となるためには、以下の条件を満たしている必要があります。
- がんと診断され、且つその病名を告知されていること
- 代替医療単独で治療効果を認めたと推測されていること
- 第三者からこの研究への参加を強要されていないこと
尚、この研究へ参加するにあたって、年齢、性別、がんの種類は問いません。
② 二次書類審査
一次書類審査において、有効性の可能性が認められ場合、画像検査のデータや病理診断の結果など提出してもらい代替医療の治療効果の評価を判定
③
データベースの作成
二次書類審査において治療効果が審査基準を満たしていた場合、医療情報を電子データ化してデータベースとして情報を蓄積
④
データの解析
効果の認められた特定の代替医療の治療法に関して、情報が蓄積された時点で臨床試験を行うことが可能かどうか検討
![]()
|
なお、当該研究において審査の対象となったことが、がん治療としての効果を認めたことを意味しているわけではありません。その治療法の効果を評価するためには、よくデザインされた臨床試験でなされる必要があり、当該研究で集められた情報は、今後の臨床試験実施に向けた基礎資料としての位置づけとなります。 |


