手術療法
手術には腎摘除術と腎部分切除術があり、それぞれの手術に開腹手術と腹腔鏡手術があります。
腎摘除術は、腎動脈と腎静脈を結紮して腎をすべて取り出す手術です(場合によっては副腎も取り出します)。一方、腎部分切除術は、腫瘍の部分のみを切り取り、腎臓を残す手術です。手術自体は腎摘除術のほうが容易で、腎部分切除術は切り取った部分からの出血や尿漏れなど、腎摘除術にはない合併症が発生する危険性があります。また、腎部分切除術では、残存腎への再発も心配されますが、4cm以下の腫瘍であれば残存腎への再発は1%程度と報告されています。
腎摘除術か部分切除術かの選択ですが、一般的に腫瘍径が7cm以下のステージⅠであれば腎部分切除術の適応になります。逆に7cmを超える腫瘍であれば腎摘除術が一般的になります。最近の研究では、腎摘除術後長期間経過すると腎機能低下をきたし、そのことに起因する合併症(たとえば心血管系の病気)での死亡率が上昇することが報告されています。腎部分切除術では腎摘除術に比較し腎機能の低下は少ないため、部分切除可能な7cm以下の腫瘍はやはり部分切除術を第一に考えるべきです。一方、7cm以下の腫瘍であっても、腫瘍が腎静脈などに浸潤している場合などには腎部分切除術が不可能な場合があります。
開腹手術か腹腔鏡手術(ロボット支援手術含む)かの基準は施設によって若干の差がありますが、やはり低侵襲手術の時代ですので可能な限り腹腔鏡で行っている施設がほとんどです。ただ、腫瘍が周囲に進行している場合や、下大静脈内に進行している場合などには通常腹腔鏡手術はできません。開腹による手術方法は腫瘍の大きさや場所により切開方法が異なります。腎摘除術の場合は正中切開が、部分切除術の場合には側臥位による腰部斜切開がよく選択されます。
腹腔鏡による手術は、トロッカーと呼ばれる5-7カ所の操作用孔(5-12mm)を介し、カメラと器具を挿入して行われます。腎摘除術の場合には腎を取り出すために5 cm程度の切開が必要になりますが、部分切除術の場合にはトロッカーのみの傷ですみます。
腎摘除術 |
腎部分切除術 |
|||
|---|---|---|---|---|
ステージが同じなら再発率、生存率は同じ |
||||
出血量、入院期間も同じ、手術時間は部分切除が長い |
||||
問題点 |
<腎機能障害> 単腎になると5年後には15%-22%腎機能が悪化するといわれている。 (クレアチニンが 2.0 以上になる) 腎障害から心血管系疾患などの他因死が多くなる |
<残存腎への再発> 1%以下と報告されているが可能性あり、 切除断端陽性や腎がんのタイプによっては再発のリスクが高くなる <腎摘には無い合併症> 切除部位からの出血・尿漏、仮性動脈瘤など 腎動脈を一時的に遮断するため腎機能が回復しない可能性あり |
||
開腹 |
腹腔鏡 |
開腹 |
腹腔鏡 |
|
長所 |
大きな腫瘍で合併切除が 必要な場合にも対応可能 |
傷が小さい(術後の痛みが少ない) 拡大された視野で手術が可能 出血が少ない |
従来からの方法 腫瘍がどこにあっても可能 |
傷が小さい(ポートの傷のみ) 拡大された視野で手術が可能、 全員がモニターで同じ視野を共有できる |
短所 |
傷が大きい(術後疼痛あり) 術後の回復がおそい |
大出血・癒着による合併切除など 不測の事態には対応困難 ポート部再発の可能性あり |
傷が大きい(術後疼痛あり) 術後の回復がおそい |
腫瘍が埋没している場合には困難 ポート部再発の可能性あり |
補足1)ロボット支援手術について
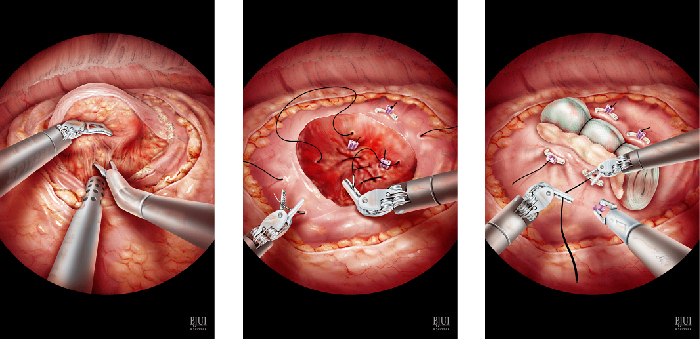
現在、腎摘除術および腎部分切除術はロボット支援手術が保険適応となっています。ロボット支援手術の特徴は、自由度の高い手術用鉗子や3次元画像により,繊細で安全な手術操作が可能であることです。このことにより従来の腹腔鏡で制限されていた欠点を補い、手術が容易になりました。特に腎部分切除術の場合、腎動脈の阻血時間短縮につながるとされています。温阻血時間短縮は腎機能温存に重要です。
補足2)
腎がんでは転移部位を手術で切除することがあります。一般にがんが転移すると手術は行われませんが、腎がんの場合、転移巣に対しても、切除可能であれば手術を検討します。全身状態が良好で転移巣が切除可能な場合には、手術により転移巣を切除することで生存期間の延長が期待されます。しかしこれは後述する薬物療法の発展により対象は限られるようになってきました。今後徐々に明らかにされてくるものと思われます。
腎がんは、進行してくると静脈内に腫瘍が進行していくことがあります。腎静脈から下大静脈、心臓まで広がる場合もあります。このように進行していても転移を認めない場合には、手術により生存率の延長が期待されるため全身状態が良好であれば手術をします。しかし、腫瘍塞栓の程度に応じて血行バイパス術の併用や人工心肺装置の使用が必要となり、術中の侵襲や危険性が高くなるため、手術適応には慎重な判断が必要となります。
腎がんの治療は手術が中心になりますが、全身状態により手術が困難な場合や、手術を拒否した場合などに低侵襲な経皮的局所療法が考慮されることがあります。経皮的局所療法には、ラジオ波焼灼術(RFA:radiofrequency ablation)と凍結療法があります。ラジオ波焼灼術はラジオ波を用いて腫瘍を高温にすることで、凍結療法は逆に低温にすることでがん細胞を破壊します。これらの治療は当院では行っていないため、他院へ紹介することになります。
薬物療法
近年、がん細胞と正常細胞の構造の違いやがん細胞の増殖のパターンなどが徐々に明らかとなってきています。がん細胞において、その特徴となっている部分、すなわち増殖や進行に関係する分子をターゲットにして開発されたのが分子標的薬剤です。理論的には、がん細胞にだけ作用して、正常細胞への影響は少ないはずです。しかしながら、実際にはこれまでに無かったような副作用が出現し、中には重篤な副作用も発症することがわかりました。2008年に分子標的薬が本邦でも認可されましたが、それまで転移のある腎がんの治療は、インターフェロンなどの免疫療法しかありませんでした。免疫療法の有効率は低く、生存に関する有益性も低いままでしたので、分子標的薬の出現により転移のある腎がんの治療は大きく様変わりしました。現在腎がんに対しては8種類の分子標的薬が使用可能です。
また、がんと免疫に関する研究が進み、これまでとは異なる作用を持つ免疫療法が開発されました。その新しい免疫療法は「免疫チェックポイント阻害療法」と呼ばれております。免疫チェックポイント阻害薬は腎癌に対して2016年8月より本邦でも認可されました。がん細胞は免疫の攻撃対象になることを防ぐための機能を持っており、がん細胞は免疫の働きにブレーキをかけてその攻撃から逃れています。従来の免疫療法は患者さん自身の免疫の力を高める療法で車の運転に例えるとアクセルをさらに踏む治療法といえます。「免疫チェックポイント阻害療法」はがんによってかけられたブレーキを外すことで患者さん自身の免疫機能を回復させて、がん細胞への攻撃力を高める新しい治療法です。
さらに、近年は分子標的薬や免疫チェックポイント阻害薬を2種類組み合わせることで、がんに対する攻撃力をさらに高める治療法が開発されました。
使用できる薬剤は増えましたが、これら薬剤による治療は組織型とリスク分類によって決まります。
リスクグループについて
IMDC(International Metastatic RCC Database Consortium)リスク分類の予後因子(KPS 80%未満、診断から治療開始までの期間が1年未満、ヘモグロビンが基準値下限未満、補正カルシウム値が基準値上限を超える、好中球絶対数が基準値上限を超える、血小板絶対数が基準値上限を超える)のうち1つも満たさない患者さんは低リスク、1~2個を満たす患者さんは中間リスク、3~6個を満たす患者さんは高リスクに分類されます。
(KPS:Karnofsky performance status, KPS 80%未満とは正常の活動・労働ができない状態です)
淡明細胞がん
組織型および治療ライン |
リスク分類 |
標準治療 |
他の治療 |
|---|---|---|---|
ファーストライン治療 |
低リスク |
インライタとキイトルーダの併用療法 カボメティクスとオプジーボの併用療法 レンビマとキイトルーダの併用療法 |
インライタとバベンチオの併用療法 カボメティクス ヴォトリエント スーテント |
中間リスクまたは高リスク |
インライタとキイトルーダの併用療法 カボメティクスとオプジーボの併用療法 ヤーボイとオプジーボの併用療法 レンビマとキイトルーダの併用療法 カボメティクス |
インライタとバベンチオの併用療法 ヴォトリエント スーテント |
|
セカンドライン以降の治療 |
カボメティクス オプジーボ |
インライタ アフィニトール ヴォトリエント スーテントネクサバール トーリセル |
|
非淡明細胞がん
組織型および治療ライン |
選択される治療 |
他の治療 |
|---|---|---|
エビデンスの高い治療法はいまのところありません |
カボメティクス スーテント カボメティクスとオプジーボの併用療法 インライタとキイトルーダの併用療法 |
オプジーボ アフィニトール インライタ ヴォトリエント トーリセル |
- ネクサバール、アフィニトール、カボメティクス、インライタは内服薬ですので毎日服用します。スーテントも内服薬ですが、4週内服、2週休薬が基本的な内服方法です。
- トーリセルは点滴で、毎週1回を継続します。
- ヤーボイとオプジーボの併用療法では、最初の4回は2種類の薬を同じ日に3週間毎に点滴し、その後はオプジーボのみを2週間間隔で点滴します。オプジーボは問題が無ければその後4週間隔にできます。
- インライタとキイトルーダの併用療法では、インライタの内服を毎日行い、キイトルーダの点滴を3週間に1回行います。キイトルーダは問題が無ければ6週間隔に出来ます。
- インライタとバベンチオの併用療法では、インライタの内服を毎日行い、バベンチオの点滴を2週間に1回行います。
- カボメティクスとオプジーボの併用療法では、カボメティクスの内服を毎日行い、オプジーボの点滴を2週間で行い、問題がなければ4週間に1回行います。
- レンビマとキイトルーダの併用療法では、レンビマの内服を毎日行い、キイトルーダの点滴を3週間で行い問題が無ければ6週間に1回行います。
副作用について
以下の表に各薬剤の副作用をまとめました。これ以外にも頻度の少ないものが数多くあります。
薬剤 |
頻度の高いもの(10%以上) |
重篤なもの(G3 で 5%以上) |
|---|---|---|
ネクサバール |
手足症候群 57%、高血圧 34%、下痢 19%、脱毛 17%、 アミラーゼ 14%、発疹 14%、肝機能異常 11% |
手足症候群、肝機能異常 |
スーテント |
血小板減少 61%、手足症候群 37%、甲状腺機能低下 36%、 高血圧 35%、白血球減少 33% |
血小板減少、白血球減少、高血圧、 手足症候群 |
アフィニトール |
口内炎 44%、発疹 30%、貧血 28%、疲労 25%、下痢 24% |
間質性肺炎、高血糖、貧血 |
トーリセル |
発疹 59%、口内炎 57%、コレステロール 43%、食欲不振 37%、 高血糖 32% |
高血糖、口内炎、間質性肺炎、 感染症、胸水 |
インライタ |
高血圧 76%、手足症候群 71%、下痢 63%、発声障害 55%、疲労 53%、 蛋白尿 40%、甲状腺機能低下 39%、口内炎 32% |
高血圧、手足症候群、疲労、 蛋白尿、食欲不振 |
ヴォトリエント |
下痢 5%、高血圧 43%、疲労 38%、肝機能障害 35%、 悪心 34%、毛髪変色 33%、食欲不振 29%、味覚異常 22%、 手足症候群 21% |
高血圧、肝障害、疲労、下痢、 手足症候群 |
オプジーボ |
疲労 33%、掻痒症 14%、悪心 14%、下痢 12%、食欲減退 12%、 発疹 10% |
なし ※免疫関連有害事象に注意必要 |
ヤーボイ+オプジーボ |
疲労 37%、掻痒症 28%、下痢 27%、発疹 22%、悪心 20%、 リパーゼ増加 17%、甲状腺機能低下症 16% |
なし ※免疫関連有害事象に注意必要 |
キイトルーダ+インライタ |
下痢 49%、高血圧 42%、甲状腺機能低下症 32%、疲労 30%、 手足症候群 28%、肝機能障害 24%、発声障害 23%、 食欲減退 22%、悪心 21% |
なし ※免疫関連有害事象に注意必要 |
バベンチオ+インライタ |
下痢 54%、高血圧 48%、疲労 36%、手足症候群 33%、 発声障害 27%、悪心 25%、甲状腺機能低下症 24%、口内炎 22%、 食欲減退 20%、悪寒 14%、粘膜の炎症 13%、ALT増加 13%、 味覚異常 13%、発疹 12%、呼吸困難 12%、掻痒症 12%、 関節痛 12%、注入に伴う反応 12%、AST増加 11%、体重減少 11% |
下痢、高血圧、手掌足底発赤知覚不全症候群 ※その他、免疫関連有害事象に注意が必要 |
カボメティクス |
下痢 70%、疲労 53%、悪心 45%、手足症候群 43%、 食欲減退 40%、高血圧症 33%、体重減少 27%、嘔吐 24%、 味覚異常 23%、甲状腺機能低下症 21%、粘膜の炎症 19%、 発声障害 18%、AST増加 17%、無力症 16%、ALT上昇 16%、 蛋白尿 13%、発疹 13%、低マグネシウム血症 12%、貧血 12%、 消化不良 11%、筋痙縮 10% |
下痢、疲労、手足症候群、高血圧 |
レンビマ+キイトルーダ |
下痢 55%、高血圧 52%、甲状腺機能低下症 43%、 食欲減退 35%、口内炎 32%、疲労 32%、手足症候群 28%、 蛋白尿 28%、悪心 27%、発声障害 25%、発疹 22% |
下痢、間質性肺炎、副腎機能不全、嘔吐、高血圧、急性心筋梗塞 ※その他、免疫関連有害事象に注意が必要 |
以上のように、各薬剤にはそれぞれ特徴があり、また出現する副作用も違います。また、欧米人と日本人とで副作用の出現率が異なることにも注意が必要です。
採血などにより、異常の早期発見に努めますが、何かあればすぐにお知らせください。患者さんからの情報が合併症の早期発見のために重要です。早期発見できれば適切な対応策がとれ、重症化せずにすみます。
また、現在内服中の薬に飲み合わせの悪い薬もありますので、薬剤師が確認します。
(2024年10月更新)




